Fetcroja® è una cefalosporina siderofora con elevata attività in vitro in
A. baumannii, P.aeruginosa e Enterobacterales resistenti ai carbapenemi compresi KPC, OXA-48 e MBL (NDM, IMP e VIM).1
L’efficacia e la sicurezza clinica di Fetcroja® sono state valutate in tre studi clinici randomizzati.2-4
In particolare, nello studio APEKS-NP Fetcroja® è stato ben tollerato; il profilo di sicurezza è coerente con quello di altre cefalosporine o carbapenemi.2
Copertura antimicrobica
Attività dei nuovi farmaci contro i patogeni Gram-negativi.5
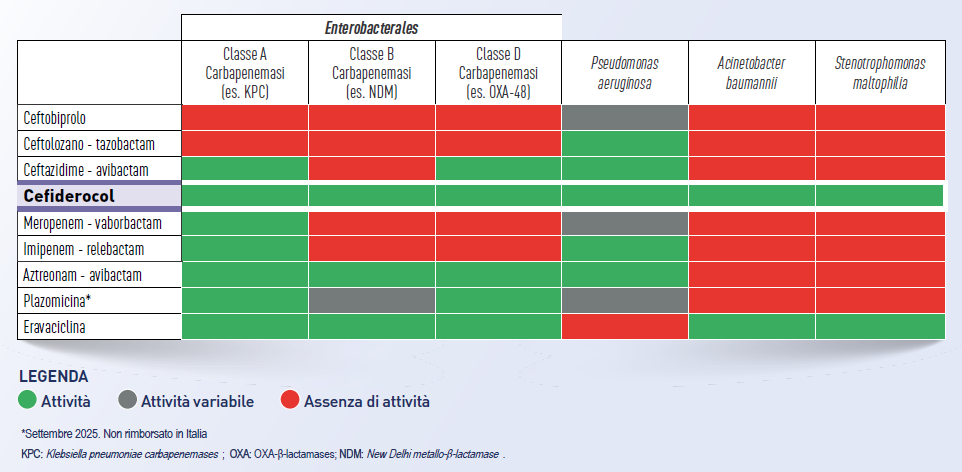
Elaborazione grafica di Figura 1, ref. 5
Posologia
Si raccomanda di utilizzare Fetcroja® per il trattamento di pazienti che dispongono di opzioni terapeutiche limitate solo previo consulto con un medico in possesso di adeguata esperienza nella gestione delle patologie infettive.6

Dose raccomandata di Fetcroja®* per i pazienti con clearance della creatinina (CrCL) ≥ 90 mL/min**
*Da usare in associazione con agenti antibatterici attivi nei confronti dei patogeni anaerobi e/o dei patogeni gram positivi, qualora sia accertato o si sospetti un loro coinvolgimento nel processo infettivo.6 **Calcolata con la formula di Cockcroft-Gault.6 *** Ad esempio, per le infezioni complicate delle vie urinarie, inclusa pielonefrite, e le infezioni intra-addominali complicate la durata del trattamento raccomandata è compresa tra 5 e 10 giorni. Per la polmonite nosocomiale, inclusa la polmonite associata a ventilazione, la durata del trattamento raccomandata è compresa tra 7 e 14 giorni. Può essere richiesto un trattamento fino a 21 giorni.6
Tabella 1, ref. 6
Tollerabilità e sicurezza
L’efficacia e la sicurezza clinica di Fetcroja® sono state valutate in tre studi clinici randomizzati. 2-4
Il profilo di sicurezza è risultato sovrapponibile ai regimi terapeutici utilizzati nei gruppi di controllo. 2-4
Le reazioni avverse più comuni sono state diarrea (8,2%), vomito (3,6%), nausea (3,3%) e tosse (2%).6
Tabella delle reazioni avverse
| Classificazione per sistemi e organi | Comune (≥1/100, <1/10) |
Non comune (≥1/1 000, <1/100) |
Non nota |
|---|---|---|---|
| Infezioni ed infestazioni |
Candidiasi incluse candidiasi orale, candidiasi vulvovaginale, candiduriae infezione da candida, colite da Clostridioidesdifficile incluse colite pseudomembranosa e infezione da Clostridioides difficile |
||
| Patologie del sistema emolinfopoietico |
Neutropenia |
||
| Disturbi del sistema immunitario |
Ipersensibilità, inclusi reazioni cutanee e prurito |
||
| Patologie respiratorie, toraciche e mediastiniche |
Tosse |
||
| Patologie gastrointestinali |
Diarrea, nausea, vomito |
||
| Patologie della cute e del tessuto sottocutaneo |
Eruzione cutanea incluse eruzione cutanea maculare, eruzione maculo papulare, esantema eritematoso ed eruzione da farmaci |
||
| Patologie renali e urinarie |
Cromaturia |
||
| Patologie sistemiche e condizioni relative alla sede di somministrazione |
Reazione in sede di infusione inclusi dolore in sede di infusione, dolore in sede di iniezione, eritema in sede di infusione e flebite in sede di iniezione |
||
| Esami diagnostici |
Alanina aminotransferasi aumentata, gamma-glutamiltransferasi aumentata, aspartatoaminotransferasi aumentata, funzione epatica anormale, inclusi test della funzionalità epatica aumentato, enzima epatico aumentato, transaminasi aumentate e test di funzionalità epatica anormale, creatinina ematica aumentata |
Urea ematica aumentata |
Tabella 3, ref. 6
Controindicazioni
Ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti.
Ipersensibilità a qualsiasi medicinale antibatterico a base di cefalosporina.
Ipersensibilità severa (ad esempio, reazione anafilattica, reazione cutanea severa) a qualsiasi altro tipo di agente antibatterico beta-lattamico (ad esempio, penicilline, monobattami o carbapenemi).6
Dati clinici
L’efficacia e la sicurezza clinica di Fetcroja® sono state valutate in tre studi clinici randomizzati. 2-4
APEKS-cUTI
In 452 pazienti adulti ricoverati in ospedale affetti da cUTI con o senza pielonefrite o pielonefrite acuta non complicate a rischio di MDR vs imipenem/cilastatina.4
Fetcroja® ha dimostrato la non inferiorità vs imipenem-cilastatina nelle cUTI.4
APEKS-NP2
In 292 pazienti adulti affetti da polmonite HAP/VAP/HCAP causata da patogeni Gram-negativi vs meropenem a dose elevata (HD).2
Fetcroja® in monoterapia si è dimostrato non inferiore alla monoterapia con meropenem HD in infusione prolungata nella mortalità per tutte le cause al giorno 14, in pazienti in condizioni critiche con polmonite nosocomiale causata da un ampio range di batteri Gram-negativi, inclusi A baumannii, P aeruginosa ed Enterobacterales.2
Fetcroja® è stato ben tollerato; il profilo di sicurezza è coerente con quello di altre cefalosporine o carbapenemi.2
CREDIBLE-CR3
In 152 pazienti adulti ricoverati in ospedale con HAP/VAP/HCAP, cUTI o infezione ematica (BSI)/sepsi causate da patogeni Gram-negativi CR vs migliore terapia disponibile.3
Fetcroja® ha dimostrato efficacia nei confronti delle infezioni potenzialmente letali, comprese quelle causate da patogeni Gram-negativi resistenti ai carbapenemi.3
Gli eventi avversi erano largamente sovrapponibili nei due gruppi di trattamento.3
Codice deposito aziendale: PP-IT-FDC-0147.
Pubblicità rivolta ai medici specialisti e farmacisti ospedalieri depositata in AIFA il: 14/05/2025.
VIETATA LA DISTRIBUZIONE/ESPOSIZIONE AL PUBBLICO
BSI: infezione del sangue; CR: carbapenem resistant; CrCL: clearance della creatinina; cUTI: infezione complicata del tratto urinario; HAP: polmonite nosocomiale; HCAP: polmonite associata al sistema sanitario; HD: dose elevata; IMP: imipenemasi; KPC: K. pneumoniae carbapenemases; MBL: metallo-β-lactamase; MDR: multidrug resistant; NDM: New-Delhi metallo-β-lactamase;OXA: OXA-β-lactamases; VIM: Verona integron-encoded metallo-β-lactamase; VAP: polmonite associata alla ventilazione meccanica.
BIBLIOGRAFIA:
- Kirkegaard-Biosca C,et al. Antibiotics (Basel). 2024;13(9):874.
- Wunderink RG, et al. Lancet Infect Dis. 2021;21(2):213-225.
- Bassetti M, et al. Lancet Infect Dis. 2021; 21 (2): 226-240
- Portsmouth et al. The Lancet Infectious Diseases.2018; 18 (12): 1319-1328.
- Bassetti M, et al. Eur Respir Rev. 2022;31(166):220119.
- Fetcroja - Riassunto delle Caratteristiche di Prodotto.
